Introdução
A osteoporose é uma doença silenciosa que afeta principalmente mulheres na pós menopausa. O desfecho clínico mais importante é a ocorrência de fraturas por baixo impacto, levando a dor, deformidades, redução da qualidade e expectativa de vida (uma fratura de quadril por fragilidade leva a 20% de mortalidade, e os que sobrevivem 50% vão ter perda de autonomia após).
É uma doença evitável e tratável, mas apenas uma pequena proporção das pessoas com risco aumentado de fratura é avaliada e tratada. Afeta mais de 200 milhões de pessoas em todo o mundo
A baixa densidade mineral óssea (DMO), especialmente no colo femoral é um forte preditor de fraturas. A cada redução de um desvio padrão na DMO, o risco de fratura aumenta em duas a três vezes. O exame de referência para a medida da DMO é a absorciometria radiológica de dupla energia (DXA – densitometria óssea)
Triagem de osteoporose
Realizar avaliação clínica de osteoporose em mulheres acima de 50 anos de idade e densitometria óssea em mulheres acima de 65 anos. Caso apresente fatores de risco para OP associado realizar a avaliação clínica antes.
Avaliação de fatores de risco:
Avaliação da DMO pode ser melhorada pela consideração concomitante de fatores de risco clínicos que operam independentemente da DMO.
– O baixo índice de massa corporal (IMC) é um fator de risco significativo para fratura de quadril.
– Uma história de fratura anterior, particularmente se causada por trauma de baixo impacto e em um local característico para osteoporose (colo femoral, coluna vertebral, antebraço distal, úmero próxima), é um importante fator de risco para novas fraturas.
Após uma fratura, o risco de fratura subsequente é maior no intervalo pós-fratura imediato (primeiro ano).
– História familiar de fratura de quadril (fator de risco independente da DMO)
– Tabagismo.
– A terapia oral com glicocorticóides aumenta o risco de fratura de maneira dose-dependente (pode ocorrer independente da DMO).
Além dos glicocorticóides, vários medicamentos são conhecidos por aumentar o risco de fratura de quadril, incluindo excesso de hormônio tireoidiano, inibidores da aromatase para o tratamento do câncer de mama e privação de andrógenos para o tratamento do câncer de próstata , tiazolidinedionas, usadas no tratamento do diabetes tipo II.Vários outros medicamentos têm sido associados ao aumento do risco de fratura, incluindo antidepressivos, antiparkinsonianos, antipsicóticos, ansiolíticos, benzodiazepínicos, sedativos, antagonistas dos receptores H2 e inibidores da bomba de prótons.
-A ingestão de álcool mostra uma relação dose-dependente com o risco de fratura (3 ou mais unidades diárias).
-Diabetes mellitus (tipo I e tipo II) está associado a um aumento no risco de fraturas de quadril e não vertebrais (duração mais longa de doença e uso de insulina estão associados a um risco aumentado).
Diagnóstico de osteoporose
O diagnóstico de osteoporose pode ser realizado se:
– Fratura por fragilidade óssea na ausência de outros distúrbios ósseos
– Densitometria óssea com T score de -2,5 ou inferior em coluna lombar/colo femoral/fêmur total/radio distal para mulheres na pós menopausa e homens acima de 50 anos.
– FRAX alto risco (acima do limiar de intervenção terapêutico).

Quando realizar o diagnóstico de osteoporose avalie causas se existe causas secundárias associadas e presença de fraturas vertebrais assintomáticas. Inicie tratamento farmacológico específico para osteoporose.
Densitometria óssea
Os resultados da densidade óssea são relatados como gramas de mineral por centímetro quadrado de área óssea projetada e são convertidos em escores T e Z.
O escore T representa o número de desvios padrão (DPs) dos valores médios normais de jovens adultos, enquanto o escore Z representa o número de desvios padrão do valor médio normal para idade, raça ou etnia e sexo.
A OMS definiu critérios de T-score para a classificação da osteoporose (T-score igual ou inferior a −2,5) e baixa DMO (ou seja, baixa massa óssea ou “osteopenia”; T-score entre -1,0 e -2.5).
Z-scores são recomendados para mulheres na pré-menopausa, com Z-score −2,0 ou inferior definido como “abaixo do intervalo esperado para a idade” e superior a -2.0 definido como “dentro da faixa esperada para a idade”.
Mulheres na pós-menopausa com escores Z muito baixos geralmente têm osteoporose secundária e devem ser submetidas a uma avaliação abrangente para essas causas
Além de seu papel no diagnóstico, a medida da DMO é útil no monitoramento da resposta à terapia.
A DXA da coluna lombar e do fêmur proximal (quadril) fornece medições de BMD precisas e reprodutíveis em locais importantes de fratura associada à osteoporose. Idealmente, ambos os quadris devem ser inicialmente medidos para evitar erros de classificação e ter uma linha de base para ambos os quadris, caso ocorra uma fratura ou substituição em um quadril.
O 1/3 distal do rádio também pode ser usado como local de diagnóstico, principalmente quando outros locais preferenciais não estiverem disponíveis.
O uso de outras sub-regiões dentro do fêmur proximal (trocânter de Ward) ou de uma vértebra individual não foi validado e não é recomendado.
Os resultados comparativos mais confiáveis são obtidos quando o mesmo instrumento e, idealmente, o mesmo tecnólogo são usados para medições seriadas.
Os resultados da DMO devem ser combinados com outros fatores de risco clínicos para fraturas para uma avaliação precisa do risco de fratura e para orientar as decisões de tratamento.
Avaliação técnica da densitometria
Situações que podem gerar erros na avaliação da densitometria óssea:
Erro de posicionamento (do paciente bem como da região de interesse), conhecimento inadequado de como eliminar vértebras fraturadas/osteoatrite, relatório impreciso de resultados e falha em comparar resultado anterior realizado em outro equipamento
Para DMO da coluna lombar L1–L4 deve ser medido, excluindo as vértebras que são afetados por alteração estrutural local ou artefato, usando pelo menos 2 vértebras para classificação diagnóstica. Vértebras anatomicamente anormais podem ser excluídas da análise se houver uma diferença de mais de 1,0 T-score entre a vértebra em questão e as vértebras adjacentes.
Cada aparelho de densitometria óssea precisa calcular o seu limite de mudança não clinicamente significativo (LSC), ou seja, caso apresente uma alteração dentro desse limite entre um exame e outro não é considerada clinicamente significativa (não é estatisticamente significativa). Valor absoluto em grama por centímetro quadrado é preferível ao uso de % (não deve exceder 5,3% para a coluna lombar, 5,0% para o quadril total e 6,9% para o colo femoral).
Escore ósseo trabecular
O escore ósseo trabecular (TBS) é um índice de textura que mede as variações do nível de cinza na imagem DXA da coluna lombar, fornecendo um índice indireto da microarquitetura trabecular. O TBS é obtido usando software que é instalado na máquina de densitometria .
Valores altos de TBS (TBS não tem unidade) se correlacionam com textura óssea homogênea (ou seja, normal), enquanto valores baixos são indicativos de textura óssea mais variável (ou seja, mais fraca). O TBS prediz o risco de fratura independente da DMO. O ajuste TBS no FRAX foi validado em coortes internacionais. A idade altera substancialmente o impacto do TBS no risco estimado do FRAX, sendo o efeito do TBS no risco de fratura muito maior para mulheres mais jovens.
Ferramenta para avaliação do risco fratura
A abordagem recomendada para a tomada de decisão é baseada em probabilidades de fratura derivadas do FRAX e pode ser aplicada a homens e mulheres com mais de 40 anos de idade.
O risco de fratura deve expresso como risco absoluto, ou seja, probabilidade em um intervalo de dez anos.
A avaliação do FRAX não leva em consideração o tratamento prévio com medicamentos para osteoporose ou a dose de vários fatores de risco clínicos sendo necessário um julgamento clínico para interpretar os resultados do FRAX.
Clique aqui para saber mais detalhes sobre FRAX.
Avaliação do risco de fratura
– Muito alto risco
Fratura recente (por exemplo, nos últimos 12 meses); fraturas durante a terapia para osteoporose; fraturas múltiplas; fraturas durante o uso de droga que cause dano esquelético (por exemplo, glicocorticóides); T score muito baixo (por exemplo, menor que -3.0); alto risco de quedas ou histórico de quedas com lesões.
– Demais pacientes com diagnóstico de osteoporose são considerados como alto risco.
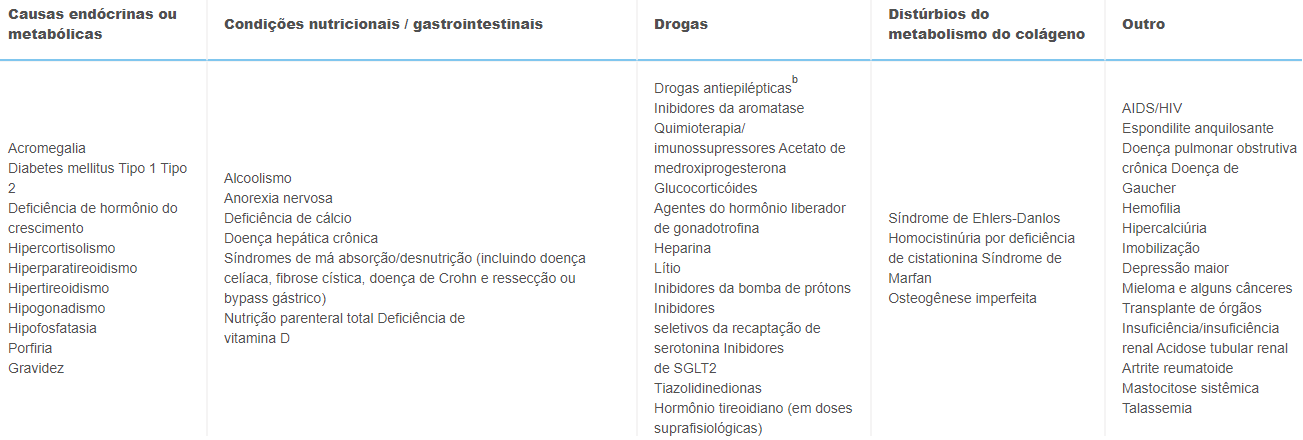
Investigação de causas secundárias
A avaliação diagnóstica de indivíduos com osteoporose deve excluir doenças que mimetizam a osteoporose, identificar a(s) causa(s) da osteoporose e incluir o manejo de qualquer comorbidade associada.
Inicial: Anamnese e exame físico (incluindo altura e avaliação da cifose torácica), hemograma, VHS/PCR, cálcio sérico, albumina, creatinina, fosforo , fosfatase alcalina, transaminases hepáticas, vitamina D, testes de função da tireoide.
Investigação se necessário: eletroforese de proteína sérica, imunoglobulinas séricas, hormônio paratireoidiano (PTH), testosterona sérica, TSH, FSH, teste de supressão de cortisol, prolactina, magnésio, anticorpos transglutaminase tecidual/anticorpos endomísios (triagem de doença celíaca), excreção urinária de cálcio, marcadores de remodelação óssea, cintilografia óssea.
Avaliação de fratura vertebral
A maioria das fraturas vertebrais atualmente não chega ao atendimento médico, e portanto, permanece sem diagnóstico (forte fator de risco para novas fraturas). A avaliação de fraturas vertebrais deve, portanto, ser considerada em indivíduos de alto risco, usando radiografias da coluna lombar e torácica lateral ou imagem DXA da coluna lateral.
Encaminhamento ao especialista
Necessidade de identificar o subgrupo de pacientes com risco de fratura muito alto que potencialmente se beneficiaria da revisão clínica por um especialista em osteoporose e que poderia se beneficiar do tratamento com drogas anabolizantes.
Quando a densidade mineral óssea é inesperadamente baixa ou quando a osteoporose tem características incomuns; quando um paciente tem uma condição que complica o manejo (por exemplo, função renal diminuída, hiperparatireoidismo ou má absorção).
Tratamento não farmacológico
Mulheres na pós-menopausa e homens com idade ≥ 50 anos, com osteoporose ou com risco de fratura por fragilidade são recomendados :
– Dieta saudável; ingestão adequada de cálcio, preferencialmente pela dieta (700 -1200 mg/dia); vitamina D (800 – 2000 UI/dia, para manter em níveis de 30 a 50 ng/ml), exercício físico (fortalecimento muscular), cessar tabagismo, restrição da ingesta de álcool (menos de 2 unidades por dia), avaliar risco de queda.
Tratamento farmacológico
Os fármacos antirreabsortivos inibem principalmente a reabsorção óssea osteoclástica com efeitos secundários posteriores na formação óssea. Drogas anabolizantes estimulam principalmente a formação óssea osteoblástica com efeitos variáveis na reabsorção óssea.
A maioria dos medicamentos se enquadra em uma ou outra categoria, mas o romosozumabe tem uma dupla ação, estimulando a formação óssea e inibindo a reabsorção óssea.
A avaliação do risco de fratura, a adequação, preferência do paciente e a relação custo-benefício devem guiar a escolha do tratamento medicamentoso.
Na maioria das pessoas com risco de fratura por fragilidade, a terapia antirreabsortiva é a opção de primeira linha
- Antirreabsortivas
1A) Bisfosfonato:
– Alendronato: 70 mg uma vez por semana por via oral é recomendado para o tratamento de mulheres com osteoporose pós-menopausa (PMO), homens com osteoporose e osteoporose induzida por glicocorticóides (GIO). Em mulheres na pós-menopausa com osteoporose, o alendronato demonstrou reduzir fraturas vertebrais, não vertebrais e de quadril.
O alendronato deve ser tomado após um jejum noturno e pelo menos 30 minutos antes da primeira comida ou bebida (exceto água) do dia. Os pacientes não devem se deitar por 30 minutos após tomar o comprimido
Efeitos colaterais: sintomas gastrointestinais superiores, distúrbios intestinais, dores de cabeça e dores musculoesqueléticas.
– Risedronato: 35 mg uma vez por semana por via oral é recomendado para o tratamento de PMO, homens com osteoporose e GIO. Demonstrou reduzir as fraturas vertebrais e não vertebrais
–Ibandronato: 150 mg uma vez por mês por via oral (3mg EV a cada 3 meses). Demonstrou reduzir a incidência de fraturas vertebrais. Não há dados disponíveis para mostrar a eficácia da redução do risco de fratura de quadril.
– Ácido Zoledrônico: 5 mg uma vez por ano por infusão intravenosa. PMO, homens com osteoporose e GIO. Em PMO demonstrou reduzir a incidência de fraturas vertebrais, não vertebrais e de quadril. Quando administrado logo após a fratura de quadril, homens e mulheres que receberam 5 mg de zoledronato anualmente tiveram menos fraturas clínicas e menor mortalidade 3 anos depois. Efeito colateral seria uma reação de fase aguda com sintomas semelhante a gripe; aumento na fibrilação atrial já foi relatado.
Oferecer zoledronato intravenoso como opção de tratamento de primeira linha após fratura de quadril é recomendado pelo guideline britânico.
Osteonecrose da mandíbula e fraturas femorais atípicas são efeitos colaterais que podem ocorrer com uso do bisfosfonato.
– Contraindicação aos bisfosfonatos: pacientes com hipocalcemia, hipersensibilidade aos bisfosfonatos, em mulheres grávidas ou lactantes. Os bisfosfonatos orais são contraindicados em pessoas com anormalidades do esôfago que retardam o esvaziamento esofágico, como estenose ou acalasia, e incapacidade de ficar em pé ou sentado por pelo menos 30 a 60 minutos. TGF menor que 30 ml/min.
1B) Denosumabe
Anticorpo monoclonal humano contra o Ativador do Receptor do Ligante Kappa B do Fator Nuclear (RANKL).
Está aprovado para o tratamento de PMO e homens com risco aumentado de fratura, para o tratamento da perda óssea associada à ablação hormonal em homens com câncer de próstata com risco aumentado de fratura e para o tratamento da perda óssea associada à terapia sistêmica de glicocorticoide.
Administrado por injeção subcutânea de 60mg uma vez a cada 6 meses
Demonstrou-se que reduz a incidência de fraturas vertebrais, não vertebrais e de quadril em mulheres na pós-menopausa com osteoporose, com segurança e eficácia mantida ao longo de 10 anos de tratamento.
O denosumabe é contraindicado em pacientes com hipocalcemia ou hipersensibilidade a qualquer um dos constituintes da formulação. Seu uso não é recomendado na gravidez ou em menores de 18 anos.
A ingestão adequada de cálcio e vitamina D é importante em todos os pacientes, especialmente naqueles com insuficiência renal grave.
Em pacientes predispostos a hipocalcemia (ClCr<35), os níveis séricos de cálcio também devem ser verificados dentro de 2 semanas após a dose inicial.
Os efeitos colaterais incluem infecção da pele (celulite), eczema, hipocalcemia e flatulência, osteonecrose da mandíbula e fraturas femorais atípicas.
Os pacientes que descontinuam o denosumabe têm um risco aumentado de sofrer fraturas vertebrais múltiplas.
O aumento do risco de fratura vertebral após a interrupção da terapia com denosumabe enfatiza a necessidade de considerar a continuação do tratamento com um medicamento antirreabsortivo alternativo após a retirada do denosumabe. Uma infusão intravenosa de 5 mg de zoledronato 6 meses após a última injeção de denosumabe, reduz a perda óssea subsequente.
O monitoramento dos marcadores de renovação óssea em 3 e 6 meses após a infusão de zoledronato pode ajudar a orientar o momento das infusões subsequentes. Quando os marcadores de remodelação óssea não estão disponíveis, uma segunda infusão de zoledronato após 6 meses foi proposta.
O alendronato oral 70 mg uma vez por semana mostrou manter a DMO por 12 meses na maioria dos pacientes após um ano de terapia com denosumabe.
Naqueles que tiveram mais de 3 anos de tratamento com denosumabe e interrompem o tratamento parece ter uma perda maior mesmo com a terapia de bisfosfonato após.
Antes de iniciar o denosumabe, assegure-se de que um plano personalizado de tratamento da osteoporose de longo prazo esteja em vigor e que tanto o paciente quanto o médico estejam cientes de que o tratamento com denosumabe não deve ser interrompido ou adiado sem discussão com um profissional de saúde.
1C) Terapia de reposição hormonal
Compreende formulações de estrogênio ou combinações de estrogênio mais progesterona.
Estrógenos equinos conjugados 0,625 mg diários ± 2,5 mg/dia de acetato de medroxiprogesterona demonstraram reduzir o risco de fratura vertebral, não vertebral e de quadril em mulheres na pós-menopausa.
As mulheres que usaram terapia apenas com estrogênio em comparação com placebo tiveram um risco significativamente menor de fraturas, mas um risco significativamente maior de doença da vesícula biliar, acidente vascular cerebral, tromboembolismo venoso e incontinência urinária.
Mulheres usando combinação de estrogênio com progesterona em comparação com placebo tiveram um risco significativamente menor de fraturas, mas tiveram um risco significativamente maior de câncer de mama invasivo, provável demência, doença da vesícula biliar, acidente vascular cerebral, incontinência urinária e tromboembolismo venoso.
TRH no manejo da osteoporose em mulheres: < 60 anos, que recentemente (dentro de 10 anos) entraram na menopausa, que apresentam sintomas da menopausa e têm baixo nível basal risco de eventos adversos.
1D) Calcitriol
O calcitriol (1,25-dihidroxivitamina D) é a forma ativa da vitamina D e está aprovado para o tratamento da osteoporose pós-menopáusica estabelecida na dose oral de 0,25 µg duas vezes ao dia. Reduz o risco de fratura vertebral em mulheres pós-menopáusicas com osteoporose, mas não foram demonstrados efeitos em fraturas não vertebrais e de quadril. É contraindicado em pacientes com hipercalcemia ou calcificação metastática. Os níveis de cálcio e creatinina devem ser monitorados.
1E) Raloxifeno
É um modulador seletivo do receptor de estrogênio e inibe a reabsorção óssea. É aprovado para o tratamento e prevenção da osteoporose em mulheres na pós-menopausa. Demonstrou-se que o raloxifeno reduz o risco de fraturas vertebrais, mas a redução de fraturas não vertebrais e de quadril não foi demonstrada.
Via oral em dose única diária de 60 mg e pode ser tomado a qualquer momento, independentemente das refeições. O raloxifeno é contraindicado em mulheres com potencial para engravidar, sangramento uterino inexplicável, insuficiência hepática ou renal grave e em mulheres com histórico de tromboembolismo venoso. Os efeitos colaterais incluem cãibras nas pernas, edema e sintomas vasomotores.
- Terapia anabólica
2A) Teriparatida
É um hormônio paratireoideano humano recombinante que ativa os osteoblastos e estimula a formação óssea.
Quando administrada de forma intermitente, a teriparatida tem efeitos anabólicos esqueléticos que são mais marcantes no osso trabecular.
Aprovada para o tratamento da osteoporose em mulheres na pós-menopausa, homens com risco de fratura por fragilidade e osteoporose associada à terapia com glicocorticóides. Demonstrou reduzir as fraturas vertebrais e não vertebrais em mulheres pós-menopáusicas com osteoporose. Não há dados de desfechos primários de eficácia disponíveis para incidência de fratura de quadril.
Administrada por injeção subcutânea na dose de 20 µg/dia. A duração do tratamento é limitada a 24 meses.
Contraindicada em pacientes com hipercalcemia, doenças ósseas metabólicas que não sejam osteoporose e osteogênese imperfeita, insuficiência renal grave, doença maligna que afeta o esqueleto, radiação prévia no esqueleto e em mulheres grávidas ou lactantes.
Os níveis de PTH precisam estar normais para iniciar a teriparatida.
Os efeitos colaterais incluem dor de cabeça, náusea, tontura, hipotensão postural e dor nas pernas.
2B) Romosozumabe
Anticorpo monoclonal humanizado que se liga e inibe a esclerostina.
Tem uma dupla ação, estimulando a formação óssea e inibindo a reabsorção óssea e está aprovado para o tratamento da osteoporose grave em mulheres pós-menopáusicas com risco muito elevado de fratura. Atualmente não é aprovado para uso em homens.
É administrado como uma injeção subcutânea em uma dose de 210 mg (administrada em duas injeções subcutâneas de 105 mg cada) uma vez por mês.
A duração do tratamento é limitada a 12 meses.
Romosozumabe é contraindicado em pacientes com hipocalcemia, hipersensibilidade a qualquer um dos constituintes da formulação ou história de infarto do miocárdio ou acidente vascular cerebral.
Tratamento medicamentoso para paciente com risco alto de fratura (osteoporose).
Alendronato, risendronato, ácido zoledrônico ou denosumabe são listados como escolhas iniciais pela Sociedade Americana de Endocrinologia. Como terapia alternativa o ibandronato e raloxifeno.
Tratamento medicamentoso para paciente com risco muito alto de fratura
Mulheres na pós-menopausa com osteoporose grave demonstraram eficácia antifratura superior de agentes anabolizantes esqueléticos versus drogas antirreabsortivas.
Teriparatida ou romosozumabe como uma opção de tratamento de primeira linha em mulheres na pós-menopausa com risco muito alto de fratura pela guideline britânico, já pela Sociedade Americana de Endocrinologia coloca que além dos anabólicos o uso de denosumabe ou ácido zoledrônico também como opção para esse grupo de pacientes.
Sequência de tratamento
Qualquer paciente que pare o uso de denosumabe, romosozumabe ou teriparatida requer uma estratégia de terapia sequencial geralmente envolvendo um medicamento antirreabsortivo, que deve ser planejada quando a terapia inicial é iniciada para evitar uma lacuna no tratamento.
Duração e monitoramento do tratamento
A osteoporose é uma condição de longo prazo para a qual não há cura atualmente, portanto, o tratamento e o monitoramento ao longo da vida para prevenir fraturas são frequentemente necessários.
Para o monitoramento ter uma densitometria inicial e repetir o exame a cada 1-2 anos até a estabilidade. Idealmente, o acompanhamento dos pacientes deve ser realizado na mesma instalação e com o mesmo sistema de densitometria óssea.
Considere o uso de marcadores de renovação óssea para avaliar a adesão do paciente e a eficácia da terapia. O marcador de reabsorção preferido é o CTX e o marcador de formação preferido é o P1NP. O CTX sérico deve ser coletado em jejum e, idealmente, sempre no mesmo horário da manhã.
A terapia com bisfosfonato está associada a eventos adversos raros, mas graves, notadamente fraturas femorais atípicas (AFFs) e osteonecrose da mandíbula (ONJ). A definição da duração ideal da terapia com bisfosfonato tenta garantir que o benefício na redução do risco de fratura supere esse pequeno risco.
É considerado tratamento bem-sucedido quando a densidade mineral óssea se mantém estável ou crescente, sem evidência de novas fraturas.
Para pacientes com 2 ou mais fraturas por fragilidade durante o tratamento ou perda de massa óssea significativa, são consideradas falha ao tratamento, sendo necessário considerar outra terapia medicamentosa.
A retirada do tratamento com bisfosfonato está associada a diminuição da DMO e aumento da renovação óssea após 2-3 anos para alendronato e 1–2 anos para ibandronato e risedronato. No caso do ácido zoledrônico, a retirada após 3 anos de tratamento está associada a apenas uma pequena diminuição na DMO após mais 3 anos sem tratamento.
Planeje prescrever bisfosfonato oral (alendronato, ibandronato e risedronato) por pelo menos 5 anos (se zoledrônico 3 anos) e depois reavaliar o risco de fratura.
Durações mais longas de tratamento, por pelo menos 10 anos (se zoledrônico 6 anos), são recomendadas nas seguintes situações para homens e mulheres:
- Idade ≥ 70 anos no momento em que o bisfosfonato é iniciado
- Quem tem história anterior de fratura(s) de quadril ou vertebral
- Tratado com glicocorticóides orais ≥ 7,5 mg de prednisolona/dia ou equivalente
- Que sofreram uma ou mais fraturas por fragilidade durante o tratamento (se o tratamento não for alterado).
- T score < -2,5
O término das “férias” do bisfosfonato deve ser baseado em circunstâncias individuais do paciente, como um aumento no risco de fratura, uma diminuição na densidade mineral óssea além da mudança menos significativa ou um aumento nos marcadores de remodelação óssea.
Se ocorrer uma nova fratura após a interrupção do tratamento com bisfosfonatos, reavalie usando FRAX e reinicie o tratamento.
Se o tratamento com bisfosfonatos for descontinuado e não ocorrer nova fratura, reavaliar usando FRAX após 18 meses para risedronato e ibandronato, 2 anos para alendronato e 3 anos para ácido zoledrônico para informar se o tratamento deve ser reiniciado.
Considerando que o FRAX não pode ser utilizado para avaliar a resposta ao tratamento, tem um papel na reavaliação do risco de fratura atual para determinar a necessidade de continuar ou descontinuar o tratamento.
Osteonecrose de mandíbula
A osteonecrose da mandíbula (ONM) ocorre muito raramente em pacientes que recebem terapia com bisfosfonatos ou denosumabe para osteoporose.
A incidência estimada naqueles que recebem bisfosfonatos é de 10-100/100.000 pessoas-ano de exposição em ensaios clínicos.
Os fatores de risco para ONM incluem má higiene oral, doença dentária, intervenções dentárias, tabagismo, câncer, quimioterapia e/ou terapia com glicocorticoides.
Durante a terapia com bisfosfonatos ou denosumabe, encoraje todos os pacientes a manter uma boa higiene bucal, fazer check-ups odontológicos de rotina e relatar quaisquer sintomas orais.
Naqueles com doença dentária grave que necessitam de tratamento com bisfosfonato ou denosumabe, revisão odontológica oportuna e tratamento odontológico por um cirurgião-dentista adequadamente experiente devem ser realizados antes da administração do medicamento, tendo em mente que o tratamento medicamentoso deve ser iniciado o mais rápido possível após uma fratura por fragilidade.
Durante o tratamento com bisfosfonatos ou denosumabe, embora idealmente, os pacientes devem minimizar procedimentos odontológicos invasivos sempre que possível, se indicado, eles podem ser realizados com segurança e sucesso na maioria dos pacientes. Quando procedimentos odontológicos são necessários, não há dados disponíveis para mostrar se a descontinuação do tratamento reduz o risco de ONM. O julgamento clínico do médico assistente deve orientar o plano de tratamento de cada paciente com base na avaliação individual de benefício/risco, garantindo que os pacientes continuem a ter acesso aos cuidados odontológicos de rotina.
Fratura atípica de fêmur
Principalmente das regiões subtrocantérica e diafisária do fêmur.
A raça asiática, o arqueamento femoral e o uso de glicocorticoides foram identificados como fatores de risco.
Incidência de 3,2 e 50 casos/100.000 pessoas-ano de exposição
Fraturas atípicas do fêmur são frequentemente bilaterais, associadas a dor prodrômica e tendem a cicatrizar mal. A dor prodrômica pode ser sentida na coxa, virilha ou quadril por dias, semanas ou meses antes da fratura.
A descontinuação da terapia com bisfosfonato ou denosumabe é aconselhada em pacientes que desenvolvem uma fratura atípica.
Após um AFF, se o risco de fratura por fragilidade for baixo, outros tratamentos ósseos farmacológicos podem ser evitados. Se o risco de fratura for alto e tiver sido realizada fixação cirúrgica bilateral das fraturas, considerar o uso de teriparatida. Se unilateral ou nenhuma intervenção cirúrgica ocorreu, considere teriparatida ou romosozumabe.
Homens usando terapia de privação androgênica (ADT)
Usada principalmente no tratamento de homens idosos com câncer de próstata, é frequentemente associada ao hipogonadismo.
A osteoporose causada pela ADT está associada à rápida perda de DMO dentro de 6-12 meses após o início da terapia.
Todos os homens que iniciam terapia de privação androgênica devem ter seu risco de fratura avaliado usando FRAX, considerando o uso de ADT como causa secundária de osteoporose, com DMO medida quando disponível.
Se FRAX abaixo do limiar de intervenção reavaliar 12 a 18 meses após o início da ADT.
Bisfosfonato e denosumabe são tratamentos medicamentosos eficazes para prevenir a perda de DMO em homens com câncer de próstata em uso de ADT.
Mulheres recebendo terapia com inibidor de aromatase (IA)
O uso de inibidores da aromatase (IA) em mulheres na pós-menopausa induz a perda óssea a uma taxa média de 1 a 3% ao ano em locais ricos em osso trabecular. A perda óssea é mais acentuada em mulheres jovens.
Realizar densitometria óssea de linha de base para avaliar a DMO no momento do início da terapia com IA.
Considerar o uso de AI como uma causa secundária de osteoporose no FRAX.
Reavaliar o risco 12 a 24 meses após o início da terapia com IA naquelas que o FRAX esteja abaixo do limite de intervenção.
O tratamento medicamentoso deve ser bifosfonato ou denosumabe.
Tratamento de fraturas vertebrais osteoporóticas sintomáticas
As fraturas vertebrais podem causar dor aguda e crônica, perda de altura, deformidade da coluna vertebral e redução da qualidade de vida.
A analgesia para dor aguda é importante para permitir a restauração da função e mobilidade.
Exercício supervisionado por fisioterapeuta após a fratura vertebral melhora a dor e o desempenho físico, além de reduzir o medo de quedas.
O uso rotineiro de órtese para o tratamento de fraturas vertebrais agudas ou subagudas não é ser recomendado.
A evidência atual não suporta o uso rotineiro de vertebroplastia percutânea ou cifoplastia para o tratamento de fraturas vertebrais osteoporóticas dolorosas, pois esses procedimentos não mostram benefício consistente para o paciente.
Se uma fratura vertebral estiver associada a déficits neurológicos iminentes ou existentes, é indicado o encaminhamento para serviços de cirurgia da coluna vertebral.
Quer saber mais sobre esse assunto? Entre em contato comigo!
Referências:
- Gregson, C.L., Armstrong, D.J., Bowden, J. et al.UK clinical guideline for the prevention and treatment of osteoporosis. Arch Osteoporos 17, 58 (2022).
- Pauline M. Camacho. et al. American Association of Clinical Endocrinologists/American College of Endocrinology Clinical Practice Guidelines for the Diagnosis and Treatment of Postmenopausal Osteoporosis—2020 Update. Endocrine Practice, 2020
- Lewiecki E.M.Binkley N.Morgan S.L.et al.Best practices for dual-energy X-ray absorptiometry measurement and reporting: International Society for Clinical Densitometry Guidance.J Clin Densitom.2016; 19: 127-140